右图是甲、乙两种固体物质的溶解度曲线,试回答下列相关问题。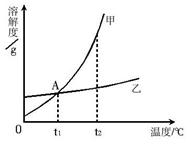
(1)t1℃时,100g水中溶解20g甲,溶液刚好饱和;那么,50g水中溶解 g乙,溶液达到饱和;
(2)t2℃时,比较两物质的溶解度大小: ;
(3)t1℃时,若要将甲物质的饱和溶液变为不饱和溶液,可采用的方法是
(写出一种即可);
(4)若要从甲中含有少量乙的混合溶液
中提纯甲,可用的方法是 。
右图是甲、乙两种固体物质的溶解度曲线,试回答下列相关问题。
(1)t1℃时,100g水中溶解20g甲,溶液刚好饱和;那么,50g水中溶解 g乙,溶液达到饱和;
(2)t2℃时,比较两物质的溶解度大小: ;
(3)t1℃时,若要将甲物质的饱和溶液变为不饱和溶液,可采用的方法是
(写出一种即可);
(4)若要从甲中含有少量乙的混合溶液
中提纯甲,可用的方法是 。