( 6分)某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示。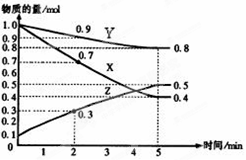
①由图中的数据分析,该反应的化学反应方程式为 ;
②反应开始至2min,Z的平均反应速率为 ;
③若不改变外界条件,5min ~ 6min Z的生成速率(V1)与6min后Z的生成速率(V2)的大小关系为:V1 V2(填大于、小于或等于)。
( 6分)某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示。
①由图中的数据分析,该反应的化学反应方程式为 ;
②反应开始至2min,Z的平均反应速率为 ;
③若不改变外界条件,5min ~ 6min Z的生成速率(V1)与6min后Z的生成速率(V2)的大小关系为:V1 V2(填大于、小于或等于)。