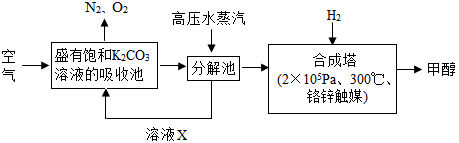
pC类似pH,是指极稀溶液中,溶质物质的量浓度的常用对数负值。如某溶液溶质的浓度为:1×10-3mol/L,则该溶液中溶质的pC=-lg1×10-3=3。下图为,H2CO3在加入强酸或强碱溶液后,平衡时溶液中三种成分的pC—pH图。请回答下列问题:
(1)在人体血液中,HCO3-能起到稳定人体PH的作用,请用电解质溶液中的平衡解释:
(用方程式表示)。
(2)H2CO3一级电离平衡常数的数值Ka1
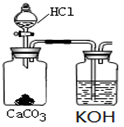
(3)某同学认为该溶液中Na2CO3的水解是微弱的,发生水解的CO32-离子不超过其总量的10%。请你设计简单实验证明该同学的观点是否正确 。
(4)已知某温度下Li2CO3的Ksp为1.68×10-3,将适量Li2CO3固体溶于100 mL水中至刚好饱和,饱和Li2CO3溶液中c(Li+)=0.15 mol·L-1。c(CO32-)=0.075 mol·L-1,若t1时刻在上述体系中加入100 mL0.125 mol·L-1 Na2CO3溶液,列式计算说明是否有沉淀产生。
(5)请画出t1时刻后Li+和CO32-浓度随时间变化关系图(用虚线表示Li+ ,实线表示CO32-)。

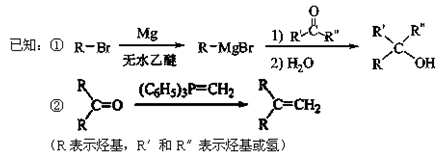
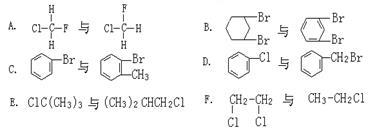
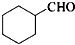 的合成路线流程图(无机试剂任用)(合成路线流程图示例如下:H2C═CH2
的合成路线流程图(无机试剂任用)(合成路线流程图示例如下:H2C═CH2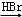 CH3CH2Br
CH3CH2Br CH3CH2OH )
CH3CH2OH )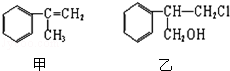
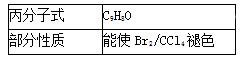
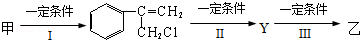

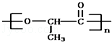 是由一种单体脱水缩聚而成的,该单体的键线式为____________
是由一种单体脱水缩聚而成的,该单体的键线式为____________ )滴入Na2CO3溶液中,生成的有机物的结构简式是:____________
)滴入Na2CO3溶液中,生成的有机物的结构简式是:____________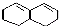 在较高温度下和Br2按物质的量之比1:1发生1,4-加成反应的化学方程式
在较高温度下和Br2按物质的量之比1:1发生1,4-加成反应的化学方程式 粤公网安备 44130202000953号
粤公网安备 44130202000953号