某学生做浓硫酸性质的实验:在一个白色的点滴板的孔穴中分别放入小纸片、少量CuSO4·5H2O。然后如图所示,分别滴入几滴浓硫酸或稀硫酸,观察现象。回答下列问题: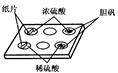
(1)浓硫酸滴入小纸片上,小纸片变 _________(填实验现象),说明浓硫酸具有_________性。
(2)稀硫酸滴入CuSO4·5H2O中,胆矾_________________(填实验现象);浓硫酸滴入CuSO4·5H2O中,胆矾_______________(填实验现象),说明浓硫酸具有_______性。
某学生做浓硫酸性质的实验:在一个白色的点滴板的孔穴中分别放入小纸片、少量CuSO4·5H2O。然后如图所示,分别滴入几滴浓硫酸或稀硫酸,观察现象。回答下列问题:
(1)浓硫酸滴入小纸片上,小纸片变 _________(填实验现象),说明浓硫酸具有_________性。
(2)稀硫酸滴入CuSO4·5H2O中,胆矾_________________(填实验现象);浓硫酸滴入CuSO4·5H2O中,胆矾_______________(填实验现象),说明浓硫酸具有_______性。