如图A 为直流电源,B为浸透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色,请填空: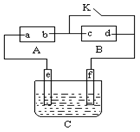
(1)电源A上的a为________极;
(2)滤纸B上发生的总化学方程式为______________________;
(3)欲在电镀槽中实现铁上镀铜,接通K点,使c、d
两点短路,则电极e上发生的反应为________________,
电极f上发生的反应为______________________,槽中放的电镀液可以是__________(填一种电解质溶液即可)。
如图A 为直流电源,B为浸透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色,请填空:
(1)电源A上的a为________极;
(2)滤纸B上发生的总化学方程式为______________________;
(3)欲在电镀槽中实现铁上镀铜,接通K点,使c、d
两点短路,则电极e上发生的反应为________________,
电极f上发生的反应为______________________,槽中放的电镀液可以是__________(填一种电解质溶液即可)。