下图为A、B、C、D、E五种物质的相互转化关系,请按如下要求填空: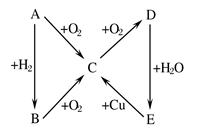
(1)若A是气体单质,则A的结构式为 ,B的电子式为 ,由D生成E的反应的化学方程式是 ;
(2)若A为固体单质,则A元素在元素周期表中的位置是在第 周期第 族,由E生成C的反应的化学方程式是 。
下图为A、B、C、D、E五种物质的相互转化关系,请按如下要求填空:
(1)若A是气体单质,则A的结构式为 ,B的电子式为 ,由D生成E的反应的化学方程式是 ;
(2)若A为固体单质,则A元素在元素周期表中的位置是在第 周期第 族,由E生成C的反应的化学方程式是 。