根据要求填空:
(1)写出下列有机物的键线式: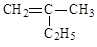 __ _____ ____ CH3CH2CH2COOH _ ________
__ _____ ____ CH3CH2CH2COOH _ ________
(2)写出有机物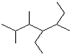 的结构简式
的结构简式
(3)[Ni(NH3)2Cl2]可以形成A、B两种固体,A在水中溶解度较大;B在CCl4中溶解度较大。试画出A、B分子的几何构型。
根据要求填空:
(1)写出下列有机物的键线式: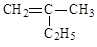 __ _____ ____ CH3CH2CH2COOH _ ________
__ _____ ____ CH3CH2CH2COOH _ ________
(2)写出有机物 的结构简式
的结构简式
(3)[Ni(NH3)2Cl2]可以形成A、B两种固体,A在水中溶解度较大;B在CCl4中溶解度较大。试画出A、B分子的几何构型。