CO和H2在一定条件下可以合成乙醇:2CO(g) + 4H2(g) 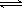 CH3CH2OH(g)+ H2O(g)
CH3CH2OH(g)+ H2O(g)
下列叙述中能说明上述反应在一定条件下已达到最大限度的是( )
| A.CO全部转化为乙醇 |
| B.正反应和逆反应的化学反应速率均为零 |
| C.CO和H2以1:2的物质的量之比反应生成乙醇 |
| D.反应体系中乙醇的物质的量浓度不再变化 |
CO和H2在一定条件下可以合成乙醇:2CO(g) + 4H2(g) 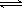 CH3CH2OH(g)+ H2O(g)
CH3CH2OH(g)+ H2O(g)
下列叙述中能说明上述反应在一定条件下已达到最大限度的是( )
| A.CO全部转化为乙醇 |
| B.正反应和逆反应的化学反应速率均为零 |
| C.CO和H2以1:2的物质的量之比反应生成乙醇 |
| D.反应体系中乙醇的物质的量浓度不再变化 |