已知25℃时,弱电解质的电离平衡常数:Ka(CH3COOH)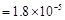 ,Ka(HSCN)
,Ka(HSCN)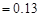 。在物质的量浓度均为
。在物质的量浓度均为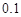 mol·L
mol·L 的CH3COONa和NaSCN混合溶液中,下列排序正确的是( )
的CH3COONa和NaSCN混合溶液中,下列排序正确的是( )
A.c(OH )>c(CH3COOH)>c(HSCN)>c(H )>c(CH3COOH)>c(HSCN)>c(H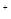 ) ) |
B.c(OH )>c(HSCN)>c(CH3COOH)>c(H )>c(HSCN)>c(CH3COOH)>c(H ) ) |
C.c(OH )>c(SCN )>c(SCN )>c(CH3COO )>c(CH3COO )>c(H )>c(H ) ) |
D.c(OH )>c(CH3COO )>c(CH3COO )>c(SCN )>c(SCN )>c(H )>c(H ) ) |
已知25℃时,弱电解质的电离平衡常数:Ka(CH3COOH)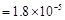 ,Ka(HSCN)
,Ka(HSCN)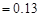 。在物质的量浓度均为
。在物质的量浓度均为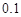 mol·L
mol·L 的CH3COONa和NaSCN混合溶液中,下列排序正确的是( )
的CH3COONa和NaSCN混合溶液中,下列排序正确的是( )
A.c(OH )>c(CH3COOH)>c(HSCN)>c(H )>c(CH3COOH)>c(HSCN)>c(H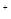 ) ) |
B.c(OH )>c(HSCN)>c(CH3COOH)>c(H )>c(HSCN)>c(CH3COOH)>c(H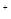 ) ) |
C.c(OH )>c(SCN )>c(SCN )>c(CH3COO )>c(CH3COO )>c(H )>c(H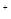 ) ) |
D.c(OH )>c(CH3COO )>c(CH3COO )>c(SCN )>c(SCN )>c(H )>c(H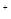 ) ) |