某校化学实验室废油桶中收集了溶有大量
的废液,此外还有一些不溶性杂质。若废液直接排放到下水道不仅造成重金属污染,而且造成浪费。该校化学兴趣小组同学设计了如下图费用处理方案,请回答有关问题。
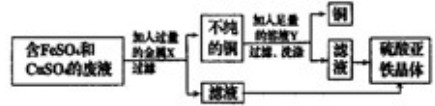
(1)废液在加入金属
前需进行过滤,目的是将其中的除去。进行过滤操作所需的玻璃仪器有:。
(2)金属
是,其加入废液后发生反应的化学方程式为;溶液
是,利用其除去铜中杂质,有关反应的化学方程式为。
某校化学实验室废油桶中收集了溶有大量
的废液,此外还有一些不溶性杂质。若废液直接排放到下水道不仅造成重金属污染,而且造成浪费。该校化学兴趣小组同学设计了如下图费用处理方案,请回答有关问题。

(1)废液在加入金属
前需进行过滤,目的是将其中的除去。进行过滤操作所需的玻璃仪器有:。
(2)金属
是,其加入废液后发生反应的化学方程式为;溶液
是,利用其除去铜中杂质,有关反应的化学方程式为。