(1)下列物质中,与CH2 =CHCH2OH属于同系物的有 ,与CH2 =CHCH2OH互为同分异构体的是 (填序号)
| A.CH3CH2OH | B.CH2 =CH—CH=CH—CH2—OH |
| C.CH3CH=CHCH2OH | D.CH3CH2CHO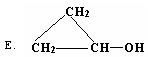 |
(2)某研究小组对铁生锈进行研究: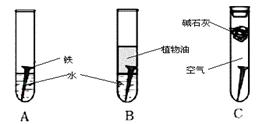
经过较长时间后,甲同学观察到的现象是: 上图中的铁钉最容易生锈的是 (填字母),铁锈的主要成分是
②根据实验条件判断,在铁钉的锈蚀过程中,正极的电极反应为
(1)下列物质中,与CH2 =CHCH2OH属于同系物的有 ,与CH2 =CHCH2OH互为同分异构体的是 (填序号)
| A.CH3CH2OH | B.CH2 =CH—CH=CH—CH2—OH |
| C.CH3CH=CHCH2OH | D.CH3CH2CHO |
(2)某研究小组对铁生锈进行研究:
经过较长时间后,甲同学观察到的现象是: 上图中的铁钉最容易生锈的是 (填字母),铁锈的主要成分是
②根据实验条件判断,在铁钉的锈蚀过程中,正极的电极反应为