为确认C6H5OH、H2CO3、CH3COOH的酸性强弱,某同学设计了如下图所示装置,一次实验即可达到目的(不必选用其他酸性物质)。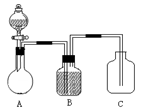
请据此实验回答下列问题:
(1)在烧瓶中装某可溶性正盐溶液,分液漏斗中所盛放的试剂应为 。
(2)装置B中所盛的试剂是 ,其作用是 。
(3)装置C中所盛的试剂是 ,C中反应的离子方程式是 。
为确认C6H5OH、H2CO3、CH3COOH的酸性强弱,某同学设计了如下图所示装置,一次实验即可达到目的(不必选用其他酸性物质)。
请据此实验回答下列问题:
(1)在烧瓶中装某可溶性正盐溶液,分液漏斗中所盛放的试剂应为 。
(2)装置B中所盛的试剂是 ,其作用是 。
(3)装置C中所盛的试剂是 ,C中反应的离子方程式是 。