下图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.试回答下列问题: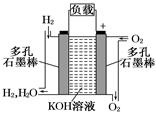
(1)图中通过负载的电子流动方向______(填“向左”或“向右”).
(2)写出氢氧燃料电池工作时电极反应方程式和总反应方程式.
负极:___________________________,总反应:________________________.
下图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.试回答下列问题:
(1)图中通过负载的电子流动方向______(填“向左”或“向右”).
(2)写出氢氧燃料电池工作时电极反应方程式和总反应方程式.
负极:___________________________,总反应:________________________.