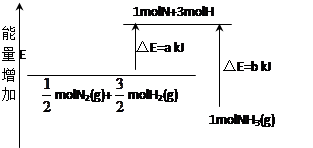(共6分)(1)已知CH4(g)+2O2 (g) = CO2 (g) +2H2O (l); △H=-890kJ/mol,现有CH4和CO共0.75mol,完全燃烧后生成CO2气体和18g液态水,并放出515kJ热量,则CO燃烧的热化学方程式为 ;
(2)化学反应N2+3H2 2NH3的能量变化如图所示,写出生成氨气时该反应的热化学方程式 。
2NH3的能量变化如图所示,写出生成氨气时该反应的热化学方程式 。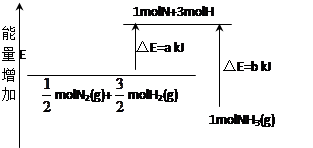
(共6分)(1)已知CH4(g)+2O2 (g) = CO2 (g) +2H2O (l); △H=-890kJ/mol,现有CH4和CO共0.75mol,完全燃烧后生成CO2气体和18g液态水,并放出515kJ热量,则CO燃烧的热化学方程式为 ;
(2)化学反应N2+3H2 2NH3的能量变化如图所示,写出生成氨气时该反应的热化学方程式 。
2NH3的能量变化如图所示,写出生成氨气时该反应的热化学方程式 。