化学能和电能的相互转化,是能量转化的重要方式之一,如图两个实验装置是实现化学能和电能相互转化的装置。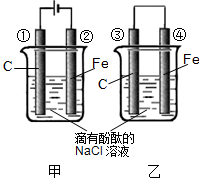
(1)把化学能转化为电能的装置是 (填“甲”或“乙”);
(2)④电极上的电极反应式为
(3)①电极上的电极反应式为 ,
检验该电极反应产物的方法是
(4)写出装置甲的反应总化学方程式 。
化学能和电能的相互转化,是能量转化的重要方式之一,如图两个实验装置是实现化学能和电能相互转化的装置。
(1)把化学能转化为电能的装置是 (填“甲”或“乙”);
(2)④电极上的电极反应式为
(3)①电极上的电极反应式为 ,
检验该电极反应产物的方法是
(4)写出装置甲的反应总化学方程式 。