在下列几种有机物中(用编号填写)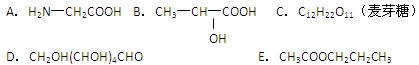
⑴既能发生银镜反应,又能发生水解反应的是 。
⑵既能与酸反应,又能与碱反应的是 。
⑶既能发生酯化反应,又能发生消去反应的是 。
⑷酸性条件下水解产物是两种相对分子质量相等的有机物是 。
在下列几种有机物中(用编号填写)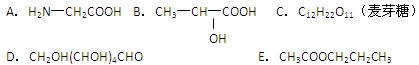
⑴既能发生银镜反应,又能发生水解反应的是 。
⑵既能与酸反应,又能与碱反应的是 。
⑶既能发生酯化反应,又能发生消去反应的是 。
⑷酸性条件下水解产物是两种相对分子质量相等的有机物是 。