请根据如图所示实验回答问题: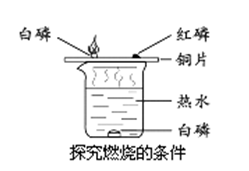
(1)该实验是通过控制温度是否达到可燃物的着火点和控制 来探究可燃物燃烧的条件。
(2)用红磷做“测定空气里氧气含量”的实验时,若红磷的量不足,所测得氧气的体积分数 (填“偏大”、“偏小”或“不变”)。该反应的化学方程式为 。
请根据如图所示实验回答问题:
(1)该实验是通过控制温度是否达到可燃物的着火点和控制 来探究可燃物燃烧的条件。
(2)用红磷做“测定空气里氧气含量”的实验时,若红磷的量不足,所测得氧气的体积分数 (填“偏大”、“偏小”或“不变”)。该反应的化学方程式为 。