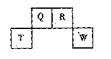
A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E 3种原子分别位于IA , IIIA , VIA族且同周期,B对应碱呈两性,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。
(1)写出下列元素符号:
A ,B ,C ,D ,E
(2)写A与E两元素可形成化合物的电子式: 。
(3)写出A、B两元素的最高价氧化物的水化物之间的相互反应的化学方程式:
。
(4) 比较C、D的最高价氧化物的水化物的酸性的强弱: 。(用化学式表示)
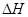 =(注:题中所设单质均为最稳定单质)。
=(注:题中所设单质均为最稳定单质)。 CH3OH(g) ΔH1
CH3OH(g) ΔH1 ,则2 mol H2生成高纯硅需_____ (填“吸收”或“放出”)能量_____ kJ。
,则2 mol H2生成高纯硅需_____ (填“吸收”或“放出”)能量_____ kJ。 粤公网安备 44130202000953号
粤公网安备 44130202000953号