化学实验室产生的废液中含有大量会污染环境的物质,为了保护环境,这些废液必须经处理后才能排放。某化学实验室产生的废液中含有两种金属离子:Fe3+、Cu2+,化学小组设计了如下图所示的方案对废液进行处理,以回收金属,保护环境。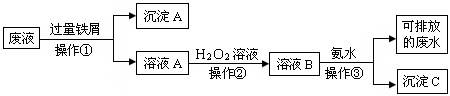
(1)操作①的名称是 。
(2)操作②反应时还需加入少量硫酸,操作②中观察到的实验现象是 。
(3)操作②中发生反应的离子方程式为 。
(4)简述以沉淀A为原料制得金属铜和绿矾晶体(FeSO4·7H2O)的实验方案。
化学实验室产生的废液中含有大量会污染环境的物质,为了保护环境,这些废液必须经处理后才能排放。某化学实验室产生的废液中含有两种金属离子:Fe3+、Cu2+,化学小组设计了如下图所示的方案对废液进行处理,以回收金属,保护环境。
(1)操作①的名称是 。
(2)操作②反应时还需加入少量硫酸,操作②中观察到的实验现象是 。
(3)操作②中发生反应的离子方程式为 。
(4)简述以沉淀A为原料制得金属铜和绿矾晶体(FeSO4·7H2O)的实验方案。