(14分)小奇同学在实验室开放日做了氧化铜和稀硫酸反应的实验后,发现实验桌上有一瓶标签残缺(如左下图所示)的NaOH溶液。为了测定此溶液的溶质质量分数,他决定利用氧化铜和稀硫酸反应后的废液。他将废液过滤,然后取100g滤液,慢慢滴加此NaOH溶液,加入NaOH溶液的质量 与生成沉淀质量的关系如右下图所示:
与生成沉淀质量的关系如右下图所示: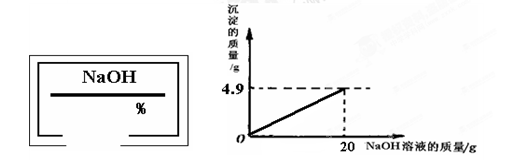
(1)计算100g滤液中CuSO4的质量;
(2)计算此氢氧化钠溶液中溶质的质量分数。
(14分)小奇同学在实验室开放日做了氧化铜和稀硫酸反应的实验后,发现实验桌上有一瓶标签残缺(如左下图所示)的NaOH溶液。为了测定此溶液的溶质质量分数,他决定利用氧化铜和稀硫酸反应后的废液。他将废液过滤,然后取100g滤液,慢慢滴加此NaOH溶液,加入NaOH溶液的质量 与生成沉淀质量的关系如右下图所示:
与生成沉淀质量的关系如右下图所示:
(1)计算100g滤液中CuSO4的质量;
(2)计算此氢氧化钠溶液中溶质的质量分数。