构成物质的微粒很多,离子就是构成物质的基本微粒之一,下表是中学化学中常见的几种离子:
回答下列问题:
(1)K+离子的结构示意图 ,Cl在周期表中的位置是 。
(2)将含OH-离子的溶液滴入浓度为0.1mol/L的Al3+和NH+4的混合溶液中,若测得溶液中NH+4减少了一半,则此时溶液中 (填“存在”或“不存在”)大量的Al3+。
(3)物质A和B分别由上表中的两种离子组成,将它们分别溶于水中,A的溶液显酸性,B的溶液显碱性且B的焰色反应呈紫色(透过蓝色钻玻璃观察),将A、B两溶液混合,既有白色沉淀生成,又有无色无味的气体生成。则A中含有的阳离子是 ,B溶液显碱性的原因是(用离子方程式和必要的文字说明) 。
(4)常温下,将(NH4)2CO3溶于水,得到含有大量NH4+和CO2-3的溶液,往溶液中滴入少量氨水,测得溶液中NH+4和CO2-3的浓度比为2:1,则此时该溶液的pH (填“<”、 “=”或“>”)7。
(5)在微生物作用下的条件,NH+4可被空气氧化成NO-3。写出该反应的离子方程式
。
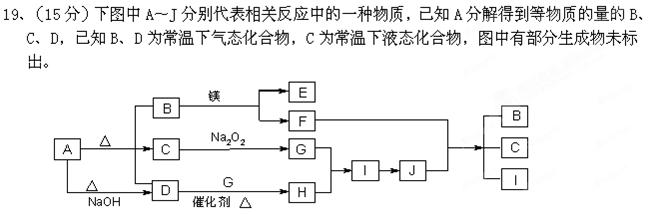
 B+镁 → E + F
B+镁 → E + F  。
。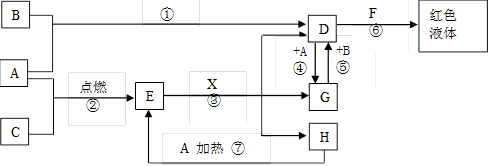

 在同周期的主族元素中原子半径最大,W是地壳中含量最多的金属元素,L的单质晶体熔点高、硬度大,是一种重要的半导体材料。用化学用语回答下列问题:
在同周期的主族元素中原子半径最大,W是地壳中含量最多的金属元素,L的单质晶体熔点高、硬度大,是一种重要的半导体材料。用化学用语回答下列问题: 种新型无机非金属材料,其化学式是。
种新型无机非金属材料,其化学式是。 _________ ______________________________________。
_________ ______________________________________。 2)另称取铁钉6.0g放入15.0ml浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。
2)另称取铁钉6.0g放入15.0ml浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。 3-、SO42-
3-、SO42- 体又有沉淀
体又有沉淀 产生;A溶液与C溶液反应只有气体产生(沉淀包括微溶物,下同)。
产生;A溶液与C溶液反应只有气体产生(沉淀包括微溶物,下同)。 粤公网安备 44130202000953号
粤公网安备 44130202000953号