下列化学符号①NO2 ②2CO ③SO4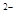 ④
④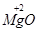 ⑤2CO3
⑤2CO3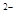 ⑥2H中数字“2”的意义:(用编号回答)
⑥2H中数字“2”的意义:(用编号回答)
(1)表示原子个数的是__________;
(2)表示分子个数的是__________;
(3)表示离子个数的是__________;
(4)表示每个分子中含有某种元素原子个数的是___________;
(5)表示一个离子所带电荷数值的是_____________;
(6)表示元素化合价数值的是___________。
下列化学符号①NO2 ②2CO ③SO4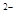 ④
④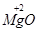 ⑤2CO3
⑤2CO3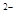 ⑥2H中数字“2”的意义:(用编号回答)
⑥2H中数字“2”的意义:(用编号回答)
(1)表示原子个数的是__________;
(2)表示分子个数的是__________;
(3)表示离子个数的是__________;
(4)表示每个分子中含有某种元素原子个数的是___________;
(5)表示一个离子所带电荷数值的是_____________;
(6)表示元素化合价数值的是___________。