高纯氧化铝可用于制高压钠灯的陶瓷管,实验室制取高纯氧化铝的流程如下: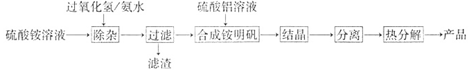
(1)“除杂”操作是加入过氧化氢后,用氨水调节溶液的pH约为8.0,以除去硫酸铵溶液中的少量Fe2+。检验Fe2+是否除尽的实验操作是 。
(2)配制硫酸铝溶液时,需用硫酸酸化,酸化的目的是 。
(3)上述流程图里,“结晶”这步操作中,母液经 得到铵明矾(含结晶水)。
(4)上述流程图里,“分离”这个步骤应包含的是 (填字母代号)
| A.蒸馏 | B.分液 | C.过滤 | D.洗涤晶体 |
高纯氧化铝可用于制高压钠灯的陶瓷管,实验室制取高纯氧化铝的流程如下:
(1)“除杂”操作是加入过氧化氢后,用氨水调节溶液的pH约为8.0,以除去硫酸铵溶液中的少量Fe2+。检验Fe2+是否除尽的实验操作是 。
(2)配制硫酸铝溶液时,需用硫酸酸化,酸化的目的是 。
(3)上述流程图里,“结晶”这步操作中,母液经 得到铵明矾(含结晶水)。
(4)上述流程图里,“分离”这个步骤应包含的是 (填字母代号)
| A.蒸馏 | B.分液 | C.过滤 | D.洗涤晶体 |