(9分)为了探究HClO的漂白性,某同学设计了如下的实验。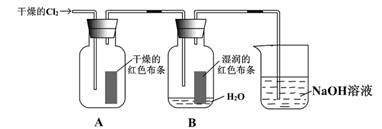
(1) 写出C12与水反应的化学方程式________________________
(2) 通入C12后,集气瓶A中的现象是__________________,集气瓶B中的现象是_______________,可得出的结论是___________________________。烧杯中的NAOH溶液的作用是 ,其反生反应的离子方程式为
(9分)为了探究HClO的漂白性,某同学设计了如下的实验。
(1) 写出C12与水反应的化学方程式________________________
(2) 通入C12后,集气瓶A中的现象是__________________,集气瓶B中的现象是_______________,可得出的结论是___________________________。烧杯中的NAOH溶液的作用是 ,其反生反应的离子方程式为