阅读下列材料后回答问题:
一个体重50kg的健康人,体内约含有2g铁,这2g铁在人体内不是以单质的形式存在,而是以Fe2+和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的Fe3+还原成Fe2+ ,有利于人体吸收。
,有利于人体吸收。
⑴
|
在人体中进行的转化时,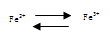 ①中的Fe2+作_____________剂,②中的Fe3+作__________剂;
①中的Fe2+作_____________剂,②中的Fe3+作__________剂;
作__________剂,具有____________性;
⑶ 市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸的作用下转
化成亚铁盐。此反应的离子方程式为_________________________________________。

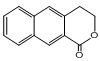 是一种重要的药物合成中间体,请结合题目所给信息,写出以
是一种重要的药物合成中间体,请结合题目所给信息,写出以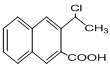 为原料制备该化合物的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
为原料制备该化合物的合成路线流程图(无机试剂任用)。合成路线流程图示例如下: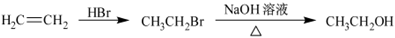
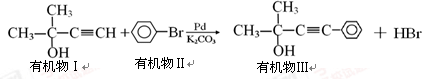
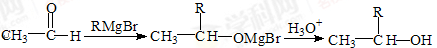
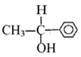 ,则需要两种有机物的结构简式分别是 。
,则需要两种有机物的结构简式分别是 。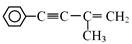 的反应方程式 。
的反应方程式 。 2NH3(g)ΔH1<0,实验Ⅰ、Ⅱ、Ⅲ中c(N2)随时间(t)的变化如图所示(T表示温度)。
2NH3(g)ΔH1<0,实验Ⅰ、Ⅱ、Ⅲ中c(N2)随时间(t)的变化如图所示(T表示温度)。


 与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物的结构简式为 。
与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物的结构简式为 。 CO(g) + 3H2(g) ΔH>0
CO(g) + 3H2(g) ΔH>0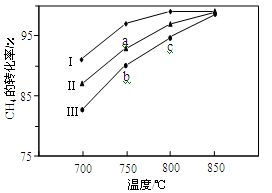
 粤公网安备 44130202000953号
粤公网安备 44130202000953号