高温下,某反应达平衡,平衡常数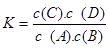 。恒容时,温度升高,B的浓度减小。下列说法正确的是
。恒容时,温度升高,B的浓度减小。下列说法正确的是
①该反应的焓变为正值 ②恒温恒容下,增大压强,B浓度一定减小
③升高温度,逆反应速率减小 ④该反应化学方程式为C(g) +D(g)  A(g)+B(g)
A(g)+B(g)
⑤增加A的量,平衡向正反应方向移动 ⑥加入催化剂,B的转化率提高
| A.①③⑥ | B.①⑤ | C.①④⑤ | D.②⑤ |
高温下,某反应达平衡,平衡常数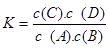 。恒容时,温度升高,B的浓度减小。下列说法正确的是
。恒容时,温度升高,B的浓度减小。下列说法正确的是
①该反应的焓变为正值 ②恒温恒容下,增大压强,B浓度一定减小
③升高温度,逆反应速率减小 ④该反应化学方程式为C(g) +D(g)  A(g)+B(g)
A(g)+B(g)
⑤增加A的量,平衡向正反应方向移动 ⑥加入催化剂,B的转化率提高
| A.①③⑥ | B.①⑤ | C.①④⑤ | D.②⑤ |