将固体NH4I置于密闭容器中,某温度下发生下列变化:
NH4I(s) 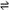 NH3 (g) + HI(g) 2HI(g)
NH3 (g) + HI(g) 2HI(g) 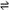 H2(g) + I2(g)
H2(g) + I2(g)
当反应达到平衡时c (H2)=" 0.5" mol/L, c (HI)=" 4" mol/L, 则 c(NH3) ,HI 的
分解率为 。
将固体NH4I置于密闭容器中,某温度下发生下列变化:
NH4I(s) 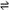 NH3 (g) + HI(g) 2HI(g)
NH3 (g) + HI(g) 2HI(g) 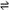 H2(g) + I2(g)
H2(g) + I2(g)
当反应达到平衡时c (H2)=" 0.5" mol/L, c (HI)=" 4" mol/L, 则 c(NH3) ,HI 的
分解率为 。