随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。
(1)目前工业上有一种方法是用CO2来生产燃料甲 醇。为探究反应原理,现进行如下实验,在体积为1 L的密闭容器中,充入1mol CO2和3mol H2,在500oC下发生反应:
醇。为探究反应原理,现进行如下实验,在体积为1 L的密闭容器中,充入1mol CO2和3mol H2,在500oC下发生反应:
CO2(g)+3H2(g)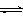 CH3OH(g)+H2O(g);△H=-49.0kJ/mol
CH3OH(g)+H2O(g);△H=-49.0kJ/mol
测得CO2和CH3OH(g)的浓度随时间变化如图所示。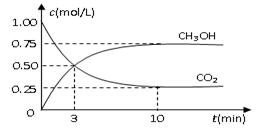
①从反应开始到平衡,氢气的平均反应速率
v(H2)=_________________________ _____;
_____;
②该反应的平衡常数K为__________ (精确到小数点后两位)。若提高温度到800oC进行达平衡时;K值__________,n(CH3OH)/n(CO2)比值__________(以上两空填“增大”、“减小”或“不变”);
(精确到小数点后两位)。若提高温度到800oC进行达平衡时;K值__________,n(CH3OH)/n(CO2)比值__________(以上两空填“增大”、“减小”或“不变”);
③平衡时CH3OH的体积分数 为__________;
为__________;
④若在相同条件下,起始时加入物质的量为:a mol CO2、b mol H2和c mol CH3OH、c mol H2O,达平衡后,CH3OH的体积分数仍为 。则a、b、c的关系为__________。
。则a、b、c的关系为__________。
(2)在载人航天器的生态系统中,不仅要求分离去除CO2,还要求提供充足的O2。某种电化学装置可实现如下转化:2CO2=2CO+O2,CO可用作燃料。已知该反应的阳极反应为:4OH―-4e―=O2↑+2H2O,则阴极反应式为_________ _____________________。
_____________________。
 H2O,则对应的两种物质是。
H2O,则对应的两种物质是。



 粤公网安备 44130202000953号
粤公网安备 44130202000953号