(10分)常温下,如果取0.1mol·L-1的HA溶液与0.1mol·L-1的NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合液的PH=8,试回答以下问题:
(1)混合溶液的PH=8的原因 (用离子方程式表示)。
(2)混合溶液中由水电离出的c(H+) 0.1mol·L-1NaOH溶液中由水电离出的c(H+)(填“>”“ <”或“=”)。
(3)求出混合溶液中下列算式的精确计算结果(填具体数字)
c(Na+)-c(A-)= mol·L-1,c(OH-)-c(HA)= mol·L-1。
(4)已知NH4A溶液为中性,又知HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的PH (填“大于”“小于”或“等于”)7;将同温度下等浓度的四种盐溶液:A、NH4HCO3 B、NH4A C、(NH4)2SO4 D、NH4Cl,按PH由大到小的顺序排列是 (填字母)。
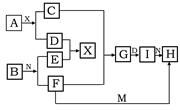
 cC(s)+dD(g)达到平衡时,其反应的K值与温度有关。请写出该反应的平衡常数表达式
cC(s)+dD(g)达到平衡时,其反应的K值与温度有关。请写出该反应的平衡常数表达式 2NO(g),这是汽车尾气中含有NO的原因之一。某同学为探究控制污染的方法,对该反应进行研究。
2NO(g),这是汽车尾气中含有NO的原因之一。某同学为探究控制污染的方法,对该反应进行研究。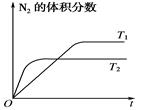
 粤公网安备 44130202000953号
粤公网安备 44130202000953号