(8分)室温下,将1.00mol/L盐酸滴入20.00mL 1.00mol/L氨水中,溶液pH和温度(0C)
随加入盐酸体积变化曲线如右图所示。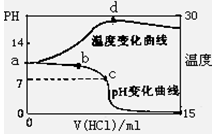
(1)下列有关说法正确的是___________
A.a点由水电离出的C(H+)=10-14mol/L
B.b点: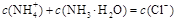
C.c点:C(Cl-)=C(NH4+)
D.d点后,容易温度略下降的主要原因是NH3·H2O电离吸热
(2)在滴加过程中,水的电离程度的变化是先 后 (填“增大”、“减小”或“不变”);
(3)在下表中,分别讨论了上述实验过程中离子浓度的大小顺序,对应溶质的化学式和
溶液的pH。试填写表中空白:
| |
离子浓度的关系 |
溶质 |
溶液的pH |
物料守恒关系 |
| ① |
C(NH4+)>C(Cl-)>C(OH-)>C(H+) |
|
pH>7 |
/ |
| ② |
|
NH4Cl |
/ |
|
| ③ |
C(Cl-)>C(H+)>C(NH4+)>C(OH-) |
|
pH<7 |
/ |
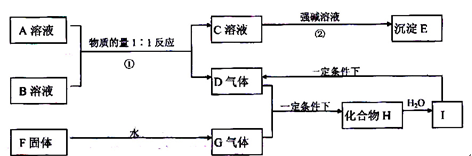
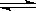 2C(g)+2D(g),
2C(g)+2D(g), 2 SO3反应。几分钟后反应达到化学平衡状态,测得容器中气体压强变为原来的90% ,则该反应达到平衡时SO2的转化率为______________。
2 SO3反应。几分钟后反应达到化学平衡状态,测得容器中气体压强变为原来的90% ,则该反应达到平衡时SO2的转化率为______________。 CO(g)+3H2(g)⊿H1="+206.1" kJ/mol
CO(g)+3H2(g)⊿H1="+206.1" kJ/mol 的物质的量浓度随反应时间的变化如图1所示。10min时,改变的外界条件可能是。
的物质的量浓度随反应时间的变化如图1所示。10min时,改变的外界条件可能是。
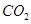 ,使甲、乙两容器初始容积相等。在相同温度下发生反应②,并维持反应过程中温度不变。已知甲容器中
,使甲、乙两容器初始容积相等。在相同温度下发生反应②,并维持反应过程中温度不变。已知甲容器中
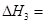 。800℃时,反应③的化学平衡常数K=1.0,某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
。800℃时,反应③的化学平衡常数K=1.0,某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
 (正)
(正) (逆) b.
(逆) b. 2SO3(g);△H=-96.56 kJ•mol-1,甲容器在反应过程中保持压强不变,乙容器保持体积不变,丙容器维持绝热,三容器各自建立化学平衡。
2SO3(g);△H=-96.56 kJ•mol-1,甲容器在反应过程中保持压强不变,乙容器保持体积不变,丙容器维持绝热,三容器各自建立化学平衡。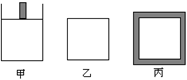
 粤公网安备 44130202000953号
粤公网安备 44130202000953号