硝酸铵是农业生产中常用的化学肥料。为测定某含有少量NaNO3的硝酸铵样品中NH4NO3的纯度,取 2.0 g 该硝酸铵样品于容器中,滴入5.0g 20%的NaOH溶液。发生如下反应:NH4NO3+NaOH=NaNO3+NH3↑+H2O。反应 过程中放出的氨气质量及加入的NaOH溶液的质量的关系如图所示:完成有关计算:
过程中放出的氨气质量及加入的NaOH溶液的质量的关系如图所示:完成有关计算: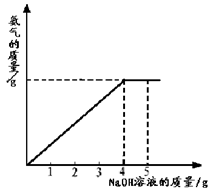
(1)NH4NO3中各元素的质量比为(H:N:O) ;
(2)样品中硝酸铵的质量分数;
(3)所得溶液中NaNO3的质量分数(保留两位小数)。
硝酸铵是农业生产中常用的化学肥料。为测定某含有少量NaNO3的硝酸铵样品中NH4NO3的纯度,取 2.0 g 该硝酸铵样品于容器中,滴入5.0g 20%的NaOH溶液。发生如下反应:NH4NO3+NaOH=NaNO3+NH3↑+H2O。反应 过程中放出的氨气质量及加入的NaOH溶液的质量的关系如图所示:完成有关计算:
过程中放出的氨气质量及加入的NaOH溶液的质量的关系如图所示:完成有关计算:
(1)NH4NO3中各元素的质量比为(H:N:O) ;
(2)样品中硝酸铵的质量分数;
(3)所得溶液中NaNO3的质量分数(保留两位小数)。