、实验室制备甲酸铜晶体[Cu(HCOO)2·4H2O]的流程如下: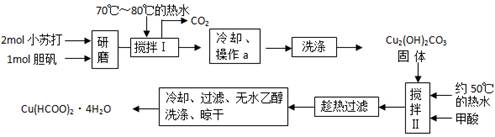
回答下列问题:
⑴小苏打和胆矾一起研磨的目的是 。
⑵生成碱式碳酸铜[Cu2(OH)2CO3]的离子方程式为 __ 。
⑶操作a的名称是 __ ,该操作使用的玻璃仪器有 __ 。
⑷证明碱式碳酸铜沉淀已经洗涤充分的实验操作方法是 __ ;
⑸“趁热过滤”的原因是 __ ;
⑹用无水乙醇洗涤晶体的目的是 __ 。
、实验室制备甲酸铜晶体[Cu(HCOO)2·4H2O]的流程如下:
回答下列问题:
⑴小苏打和胆矾一起研磨的目的是 。
⑵生成碱式碳酸铜[Cu2(OH)2CO3]的离子方程式为 __ 。
⑶操作a的名称是 __ ,该操作使用的玻璃仪器有 __ 。
⑷证明碱式碳酸铜沉淀已经洗涤充分的实验操作方法是 __ ;
⑸“趁热过滤”的原因是 __ ;
⑹用无水乙醇洗涤晶体的目的是 __ 。