已知A(g)+B(g)  C(g) +D(g) 反应过程中的能量变化如图所示,回答下列问题。
C(g) +D(g) 反应过程中的能量变化如图所示,回答下列问题。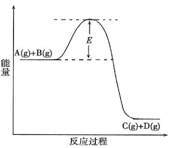
(1)该反应是_________反应(填“吸热”、“放热”)。当反应达到平衡时,升高温度,A的转化率______(填“增大”、“减小”或“不变”),
(2)在反应体系中加入催化剂,反应速率增大,E的变化是_________,(填“增大”、“减小”或“不变”)理由是 E的大小对该反应的反应热有无影响? 。
已知A(g)+B(g)  C(g) +D(g) 反应过程中的能量变化如图所示,回答下列问题。
C(g) +D(g) 反应过程中的能量变化如图所示,回答下列问题。
(1)该反应是_________反应(填“吸热”、“放热”)。当反应达到平衡时,升高温度,A的转化率______(填“增大”、“减小”或“不变”),
(2)在反应体系中加入催化剂,反应速率增大,E的变化是_________,(填“增大”、“减小”或“不变”)理由是 E的大小对该反应的反应热有无影响? 。