在2L密闭容器内,800℃时反应: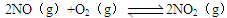 体系中,n(NO)随时间的变化如表:
体系中,n(NO)随时间的变化如表:
(1)写出该反应的平衡常数表达式:K= 。
已知:K300℃> K350℃,则该反应是 热反应。
(2)下图中表示NO2的变化的曲线是 。用O2表示从0~2s内该反应的平均速率v= 。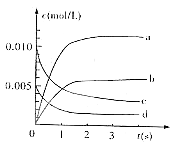
(3)下列能说明该反应已达到平衡状态的是 。
a. v(NO2)=2v(O2)
b. 容器内压强保持不变
c. v逆(NO)=2v正(O2)
d. 容器内密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是 。
a. 及时分离除NO2气体 b. 适当升高温度
c. 增大O2的浓度 d. 选择高效催化剂
 粤公网安备 44130202000953号
粤公网安备 44130202000953号