(1)化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知:N≡N键的键能是948.9 kJ/mol,H—H键的键能是436.0 kJ/mol;由N2和H2合成1 mol NH3时可 放出46.2 kJ的热量。则N—H键的键能是_______________________。
放出46.2 kJ的热量。则N—H键的键能是_______________________。
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学方程式:
Fe2O3(s)+3CO(g) = 2Fe(s)+3CO2(g) ΔH=-24.8 kJ/mol ①
3Fe2O3(s)+CO(g) = 2Fe3O4(s)+CO2(g) ΔH=-47.2 kJ/mol ②
Fe3O4(s)+CO(g) = 3FeO(s)+CO2(g) ΔH=+640 .5 kJ/mol ③
.5 kJ/mol ③
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学方程式______________________________。
(3)已知两个热化学方程式:
C(s)+O2(g)=CO2 (g) △H= ― 393.5kJ/mol
(g) △H= ― 393.5kJ/mol
2H2(g)+O2(g )=2H2O(g) △H= ― 483.6kJ/mol
)=2H2O(g) △H= ― 483.6kJ/mol
现有炭粉和H2组成的悬浮气共0.2mol,使其在O2中完全燃烧,共放出63.53kJ的热量,则炭粉与H2的物质的量之比是 .

 ,请根据化学反应的有关原理同答下列问题
,请根据化学反应的有关原理同答下列问题




 沉淀完全,而在pH≥3.2时
沉淀完全,而在pH≥3.2时
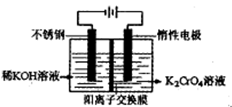
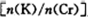 为d,则此时的铬酸钾的转化率为。
为d,则此时的铬酸钾的转化率为。 )是重要的化工原料,这种化工原料可以由玉米芯、甘蔗渣等农业废弃物水解制得,其性质见下面框图。
)是重要的化工原料,这种化工原料可以由玉米芯、甘蔗渣等农业废弃物水解制得,其性质见下面框图。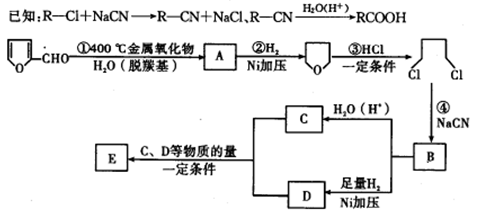
 粤公网安备 44130202000953号
粤公网安备 44130202000953号