盛极一时一种实验室常用的化学试剂,请按要求填空: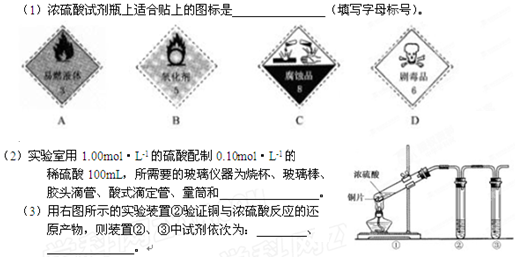
(4)装置①的反应方程式
若装置①中加入铜6.4克和含有0.2摩尔硫酸的浓硫酸产生二氧化硫
A 等于6.4克 B 大于6.4克 C 小于6.4克 D不能确定
盛极一时一种实验室常用的化学试剂,请按要求填空:
(4)装置①的反应方程式
若装置①中加入铜6.4克和含有0.2摩尔硫酸的浓硫酸产生二氧化硫
A 等于6.4克 B 大于6.4克 C 小于6.4克 D不能确定