(4分,每空2分)将下列离子Na+、K+、Cu2+、H+、NO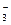 、Cl-、CO
、Cl-、CO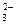 、OH-按可能大量共存于同一溶液的情况,把它们分成A、B两组,而且每组中均含两种阳离子和两种阴离子。
、OH-按可能大量共存于同一溶液的情况,把它们分成A、B两组,而且每组中均含两种阳离子和两种阴离子。
A组:________________________________ 。
B组:________________________________ 。
(4分,每空2分)将下列离子Na+、K+、Cu2+、H+、NO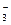 、Cl-、CO
、Cl-、CO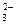 、OH-按可能大量共存于同一溶液的情况,把它们分成A、B两组,而且每组中均含两种阳离子和两种阴离子。
、OH-按可能大量共存于同一溶液的情况,把它们分成A、B两组,而且每组中均含两种阳离子和两种阴离子。
A组:________________________________ 。
B组:________________________________ 。