2008年北京残奥会吉祥物是以牛为形象设计的“福牛乐乐”(Funiulele)。有一种有机物的键线式也酷似牛形(下图所示) ,故称为牛式二烯炔醇(cowenyenynol)。回答下列有关该物质的问题:
,故称为牛式二烯炔醇(cowenyenynol)。回答下列有关该物质的问题: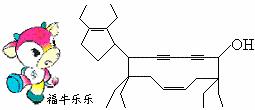
(1)“牛身”是由 个碳原子形成的碳环。
(2)1 mol牛式二烯炔醇最多可跟 mol Br2发生加成反应。
(3)该物质能否在浓硫酸、加热的条件下发生消 去反应?
去反应?
2008年北京残奥会吉祥物是以牛为形象设计的“福牛乐乐”(Funiulele)。有一种有机物的键线式也酷似牛形(下图所示) ,故称为牛式二烯炔醇(cowenyenynol)。回答下列有关该物质的问题:
,故称为牛式二烯炔醇(cowenyenynol)。回答下列有关该物质的问题:
(1)“牛身”是由 个碳原子形成的碳环。
(2)1 mol牛式二烯炔醇最多可跟 mol Br2发生加成反应。
(3)该物质能否在浓硫酸、加热的条件下发生消 去反应?
去反应?