(10分)
为测定氯化钾和硫酸钾混合物中氯化钾的含量,某同学设计了如下实验:称量样品, 溶解,添加适量A溶液,过滤,得沉淀和滤液B,将沉淀洗涤,烘干,得物质C。
溶解,添加适量A溶液,过滤,得沉淀和滤液B,将沉淀洗涤,烘干,得物质C。
回答下列问题:
(1)溶液A溶质的化学式_____,物质C的化学式____。
(2)用托盘天平称量样品,当天平平衡时,发现左盘错放砝码质量为26g,游码为0.4g,则右盘样品实际质量是____。
(3)若过滤使用的仪器和用品已有:滤纸、铁架台、铁圈、烧杯、漏斗,还需要补充的仪器或用品是______。
(4)若C的质量为23.3g,则原混合物中氯化钾的质量分数为______。


 SiHCl3+H2
SiHCl3+H2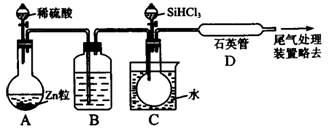
 粤公网安备 44130202000953号
粤公网安备 44130202000953号