在一定条件下,在密闭容器中反应:2NO2(g)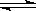 O2(g)+ 2NO(g) ΔH>0,达到
O2(g)+ 2NO(g) ΔH>0,达到 平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是
平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是
| A.当X表示温度时,Y表示NO的物质的量 |
| B.当X表示压强时,Y表示NO2的转化率 |
| C.当X表示反应时间时,Y表示混合气体的密度 |
| D.当X表示NO2的物质的量时,Y表示O2的物质的量 |
在一定条件下,在密闭容器中反应:2NO2(g)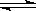 O2(g)+ 2NO(g) ΔH>0,达到
O2(g)+ 2NO(g) ΔH>0,达到 平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是
平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是
| A.当X表示温度时,Y表示NO的物质的量 |
| B.当X表示压强时,Y表示NO2的转化率 |
| C.当X表示反应时间时,Y表示混合气体的密度 |
| D.当X表示NO2的物质的量时,Y表示O2的物质的量 |