碘元素在元素周期表中的位置如图所示。放射性碘—l31(“131”是该碘原予中的质子数和中予数之和)是核反应的产物.它在衰变时产生核辐射。人服用碘片(KI)后.因吸收碘使甲状腺内的碘饱和.从而阻止放射性碘的摄入。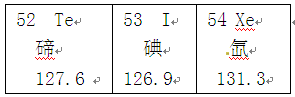
(1)碘元素的原子序数为 ;
(2)碘—l31原予与碘元素的其它原予具有相同数目的质子数,则碘—131原子中的中子数为 ;
(3)碘片中的有效成分是 元素。
碘元素在元素周期表中的位置如图所示。放射性碘—l31(“131”是该碘原予中的质子数和中予数之和)是核反应的产物.它在衰变时产生核辐射。人服用碘片(KI)后.因吸收碘使甲状腺内的碘饱和.从而阻止放射性碘的摄入。
(1)碘元素的原子序数为 ;
(2)碘—l31原予与碘元素的其它原予具有相同数目的质子数,则碘—131原子中的中子数为 ;
(3)碘片中的有效成分是 元素。