对于达到平衡的可逆反应:X+Y W+Z,增大压强则正、逆反应速率(v)的变化如图所示,分析可知X、Y、Z、W的聚集状态可能是
W+Z,增大压强则正、逆反应速率(v)的变化如图所示,分析可知X、Y、Z、W的聚集状态可能是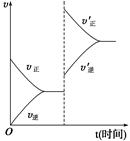
| A.Z、W为气体,X、Y中之一为气体 |
| B.Z、W中之一为气体,X、Y为非气体 |
| C.X、Y为气体,Z、W为非气体 |
| D.X、Y为气体,Z、W中至少有一种为气体 |
对于达到平衡的可逆反应:X+Y W+Z,增大压强则正、逆反应速率(v)的变化如图所示,分析可知X、Y、Z、W的聚集状态可能是
W+Z,增大压强则正、逆反应速率(v)的变化如图所示,分析可知X、Y、Z、W的聚集状态可能是
| A.Z、W为气体,X、Y中之一为气体 |
| B.Z、W中之一为气体,X、Y为非气体 |
| C.X、Y为气体,Z、W为非气体 |
| D.X、Y为气体,Z、W中至少有一种为气体 |