酸碱中和滴定是中学化学常见实验。
某同学欲测定某浓硫酸样品的物质的量浓度,进行了以下实验操作:
| A.冷却至室温后,在100mL容量瓶中定容配成100mL稀硫酸。 |
| B.量取20.00mL稀硫酸于锥形瓶中并滴入几滴指示剂。 |
C.将酸式滴定管和碱式滴定管 用蒸馏水洗涤干净,并用各待盛溶液润洗。 用蒸馏水洗涤干净,并用各待盛溶液润洗。 |
| D.将物质的量浓度为1.50mol·L-1标准NaOH溶液装入碱式滴定管,调节液面记下读数V1。 |
E.继续滴定至终点,记下读数为V2。
F.在锥形瓶下垫一张白纸,把锥形瓶移到碱式滴定管下小心滴入NaOH标准溶液,边滴边摇动锥形瓶。
G.量取浓硫酸样品5mL,在烧杯中用蒸馏水溶解。
H.重复以上实验。
请回答下列问题:
(1)操作步骤的顺序为 → A→ → →D→ → → H(用字母填写)。
(2)量取5mL浓硫酸的仪器是 ;量取20.00mL稀硫酸的仪器是 。
(3)选用的指示剂是 。
(4)判断到达滴定终点的现象是 。
(5)下表是实验测得的有关数据:
| 滴定 序号 |
待测稀硫酸 的体积(mL) |
所消耗NaOH标准溶液液的体积(mL) |
|
| V1 |
V2 |
||
| ① |
20.00 |
0.50 |
22.60 |
| ② |
20.00 |
6.00 |
27.90 |
请计算出该浓硫酸样品的浓度为 mol·L-1(不必写出计算过程)。
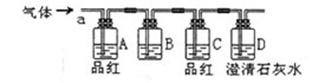

 列操作正确的是(填序号)。
列操作正确的是(填序号)。 平托盘的滤纸上,准确称量并放入烧杯中溶解后,立即注入容量瓶中
平托盘的滤纸上,准确称量并放入烧杯中溶解后,立即注入容量瓶中 mol·L-1的硫酸,注入已盛有30 mL水的100 mL的容量瓶中,加水至刻度线
mol·L-1的硫酸,注入已盛有30 mL水的100 mL的容量瓶中,加水至刻度线
 应后不久导管b出口可见到白雾,导管b段末端跟锥形瓶里液面保持一段距离的目的是___________________。
应后不久导管b出口可见到白雾,导管b段末端跟锥形瓶里液面保持一段距离的目的是___________________。 乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18 g·cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于有机溶剂,在实验室中可以用下图所示装置制备1,2—二溴乙烷。其中分液漏斗和烧瓶a中装有酒精和浓H2SO4的混合液,试管d中装有液溴(表面覆盖少量水)。填写下列空白:
乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18 g·cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于有机溶剂,在实验室中可以用下图所示装置制备1,2—二溴乙烷。其中分液漏斗和烧瓶a中装有酒精和浓H2SO4的混合液,试管d中装有液溴(表面覆盖少量水)。填写下列空白:


 粤公网安备 44130202000953号
粤公网安备 44130202000953号