右图是试验某常见气体X化学性质的实验装置,图中B为开关。若先打开B,在A处通入气体X,则C中干燥的红布条不褪色;若关闭B时,则C处干燥的红色布条褪色。回答下列问题: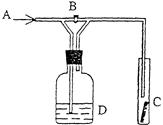
(1)气体X为
(2)D瓶中盛有的溶液可能是
A 浓H2SO4 B 饱和NaCl溶液
C 水 D 浓NaBr溶液
(3)关闭B时,C处红色布条褪色的原因是(结合必要的化学方程式解释)
右图是试验某常见气体X化学性质的实验装置,图中B为开关。若先打开B,在A处通入气体X,则C中干燥的红布条不褪色;若关闭B时,则C处干燥的红色布条褪色。回答下列问题:
(1)气体X为
(2)D瓶中盛有的溶液可能是
A 浓H2SO4 B 饱和NaCl溶液
C 水 D 浓NaBr溶液
(3)关闭B时,C处红色布条褪色的原因是(结合必要的化学方程式解释)