实验室可以用纯净的氯气和铁粉反应制取少量氯化铁固体,其反应装置示意图如下: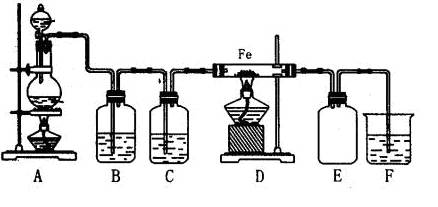
回答下列问题:
(1)A装置可制取氯气,反应前分液漏斗中药品为 ,圆底烧瓶中药品为 。
(2)写出A装置中制取氯气所发生的化学方程式是 。
(3)装置B中盛放的试剂是________________________。
(4)装置E的作用是______________________________。
实验室可以用纯净的氯气和铁粉反应制取少量氯化铁固体,其反应装置示意图如下:
回答下列问题:
(1)A装置可制取氯气,反应前分液漏斗中药品为 ,圆底烧瓶中药品为 。
(2)写出A装置中制取氯气所发生的化学方程式是 。
(3)装置B中盛放的试剂是________________________。
(4)装置E的作用是______________________________。