分别称取0.2gNaOH固体两份,加适量的蒸馏水溶解,用未知浓度的盐酸滴定,若两次所消耗盐酸的体积分别为25.02mL、24.98mL,下列说法中正确的是
A.若盐酸的浓度为0.2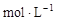 ,则第一次测出的盐酸的浓度偏高 ,则第一次测出的盐酸的浓度偏高 |
| B.若NaOH中混有少量的Na2CO3,则测定的结果偏高 |
| C.开始读数时仰视滴定管读数,滴定结束时也仰视滴定管读数,对实验结果无影响 |
| D.第二次测定的数据可能是由于滴定时不小心把盐酸滴到锥形瓶外面引起的 |
分别称取0.2gNaOH固体两份,加适量的蒸馏水溶解,用未知浓度的盐酸滴定,若两次所消耗盐酸的体积分别为25.02mL、24.98mL,下列说法中正确的是
A.若盐酸的浓度为0.2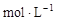 ,则第一次测出的盐酸的浓度偏高 ,则第一次测出的盐酸的浓度偏高 |
| B.若NaOH中混有少量的Na2CO3,则测定的结果偏高 |
| C.开始读数时仰视滴定管读数,滴定结束时也仰视滴定管读数,对实验结果无影响 |
| D.第二次测定的数据可能是由于滴定时不小心把盐酸滴到锥形瓶外面引起的 |