斯坦福大学B.M.Trost教授提出了绿色化学的核心概念——原子经济性。我们常用原子利用率来衡量化学反应过程的原子经济性,其计算公式为:
下面是联合工艺法制备新型自来水消毒剂ClO2,其反应原理由三步组成:
①电解氯化钠溶液NaCl+3H2O NaClO3+3H2↑
NaClO3+3H2↑
②氢气和氯气合成氯化氢
③生成二氧化氯 ↑+
↑+ ↑+
↑+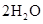
此方法的原子利用率最大为
A.37.6 B.53.6% C.62.2% D.94.4%
斯坦福大学B.M.Trost教授提出了绿色化学的核心概念——原子经济性。我们常用原子利用率来衡量化学反应过程的原子经济性,其计算公式为:
下面是联合工艺法制备新型自来水消毒剂ClO2,其反应原理由三步组成:
①电解氯化钠溶液NaCl+3H2O NaClO3+3H2↑
NaClO3+3H2↑
②氢气和氯气合成氯化氢
③生成二氧化氯 ↑+
↑+ ↑+
↑+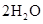
此方法的原子利用率最大为
A.37.6 B.53.6% C.62.2% D.94.4%