向足量硫酸溶液中加入100 mL 0.4 mol·L-1 Ba(OH)2溶液,放出的热量是5.12 kJ。如果向足量Ba(OH)2溶液中加入100 mL 0.4 mol·L-1HCl溶液时,放出的热量为2.2 kJ。则Na2SO4溶液与BaCl2溶液反应的热化学方程式为
| A.Ba2+(aq)+SO42-(aq)="BaSO4(s)" ΔH=-0.72 kJ·mol-1 |
| B.Ba2+(aq)+SO42-(aq)="BaSO4(s)" ΔH=-2.92 kJ·mol-1 |
| C.Ba2+(aq)+SO42-(aq)="BaSO4(s)" ΔH=-18 kJ·mol-1 |
| D.Ba2+(aq)+SO42-(aq)="BaSO4(s)" ΔH=-73 kJ·mol-1 |
 CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动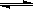 PCl5(g)
PCl5(g)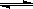 zC(g)
zC(g)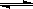 pC(气)+qD(气),若增大压强,或升高温度,重新达到平衡,
pC(气)+qD(气),若增大压强,或升高温度,重新达到平衡,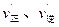 随时间化过程均如图所示,则对该反应叙述正确的是()
随时间化过程均如图所示,则对该反应叙述正确的是()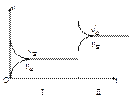
 粤公网安备 44130202000953号
粤公网安备 44130202000953号