地之都,水绿盐城!
(1)新四军纪念馆是盐城市的名片之一。馆内有许多抗战时的枪炮,但有些表面出现锈迹,
其主要原因是:铁与________、________等物质共同作用的结果。
(2)郭猛的温泉度假村是人们休闲的好去处。
①温泉水富含钾、钙、镁、氟、硅等,这里的“钾、钙、镁、氟、硅”指的是。____(填标号)
A.分子 B.原子 C.元素 D.单质
②温泉水的pH在7.5~8.9之间,该温泉水显______(填“酸性”、“碱性”或“中性”)。
③检验该温泉水是硬水还是软水的简单方法是____________________________________。

(3)新建的龙冈盐龙湖是一项重大的惠民工程,将为盐城人民提供优质水源。现在自来水的
生产过程如上图所示。
①下列属于自来水生产使用的净水方法是______。(填标号)
A.沉淀 B.过滤C.煮沸D.蒸馏
②自来水可用氯气杀菌消毒。请将下列化学方程式补充完整: Cl2 + H2O =" HClO" +________。
③能否用硝酸银区分盐城的自来水和蒸馏水_________。(填“能”或“不能”)
(4)盐城是一座以“盐”命名的城市,有着独特、深远的海盐文化,有着丰富的海水资源。以
下是我市对海水资源的部分利用。
①从海水中获得氯化钠。将海水进行可得到粗盐
②粗盐可以用过溶解、________、蒸发等操作除去其中的难溶性杂质如泥沙。
③粗盐中含有的:CaSO4、MgCl2等可溶性杂质,有如下操作:①溶解;②加过量的Na2CO3 溶液; ③加过量的BaCl2溶液;④加适量的盐酸;⑤加过量NaOH溶液;⑥蒸发结晶;⑦过滤。正确的操作顺序是。(用序号填空)
A、①⑤②③④⑦⑥ B、①③②⑤④⑦⑥ C、①③⑤②⑦④⑥
④氯化钠除食用外还是一种化工产品,如工业上利用氯化钠和水在通电条件下生成烧碱、氢气和氯气。请写出该反应的化学方程式 ________________________________________。
⑤从海水中得到金属镁。下图是从海水中提取镁的简单流程。
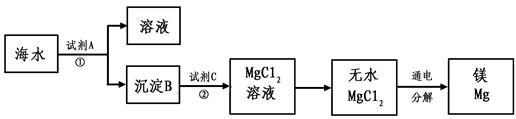
上述过程中,试剂A为熟石灰,则沉淀B为____________________。请写出沉淀B与试剂C 发生的反应的化学方程式 。

