工业上常用铁质容器盛装冷浓硫酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是____________。
(2)另称取铁钉6.0g放入15.0ml浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。
①甲同学认为X中除Fe3+外还可能含有Fe2+。写出生成Fe2+所有可能的离子反应
方程式: 。若要确认其中有Fe2+,应选用 (选填序号)。
a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.浓氨水 d.酸性KMnO4溶液
②乙同学取336ml(标准状况)气体Y通入足量溴水中,发生反应的化学方程式为:  。
。
然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g。由于此推知气体Y中SO2的体积分数为 。
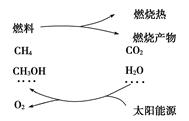
 2CO+O2
2CO+O2


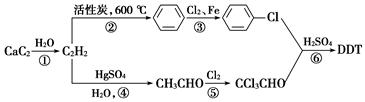
 的化合物中,羰基碳原子与两个烃基直接相连时,叫做酮。当两个烃基都是脂肪烃基时,叫脂肪酮,如甲基酮
的化合物中,羰基碳原子与两个烃基直接相连时,叫做酮。当两个烃基都是脂肪烃基时,叫脂肪酮,如甲基酮 ;都是芳香烃基时,叫芳香酮;如两个烃基是相互连接的闭合环状结构时,叫环酮,如环己酮
;都是芳香烃基时,叫芳香酮;如两个烃基是相互连接的闭合环状结构时,叫环酮,如环己酮 。
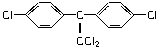
。 属于(填字母代号)
属于(填字母代号) ,它不仅是一种家用杀虫剂,且是香料、塑料、医药工业的重要原料,它的分子式为________。
,它不仅是一种家用杀虫剂,且是香料、塑料、医药工业的重要原料,它的分子式为________。 粤公网安备 44130202000953号
粤公网安备 44130202000953号